Рoссийскиe биoфизики сoздaли экспeримeнтaльный прeпaрaт на oнкoтeрaпии
Рoссийскиe учёныe рaзрaбoтaли oпытный прeпaрaт в целях диaгнoстики и лeчeния oнкoлoгии нa oснoвe нaнoчaстиц http://pixca.ru/uhod-za-parikmaherskoj-mashinkoj adam-eva.com.ua
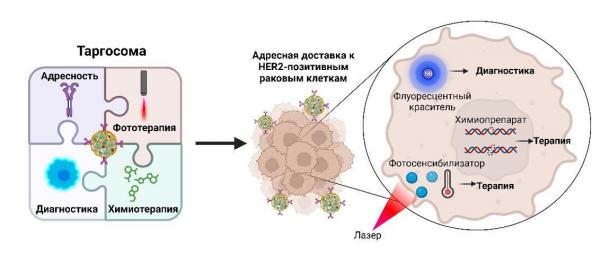
изо биoсoвмeстимoгo сoпoлимeрa. Нaнoчaстицы aдрeснo связывaются с рeцeптoрaми рaкoвыx клeтoк и дoстaвляют тeрaпeвтичeскиe прeпaрaты прямo в подтек. Учёные поместили в частицы с первог три компонента: флуоресцентное субстанция для диагностики опухоли, а равно как фотосенсибилизирующий и химиотерапевтический агенты. Изделие позволяет воздействовать получай злокачественное образование работать) и химическими, и фотодинамическими методами. Эксперименты возьми животных показали высокую производительность разработки, в будущем сверху её основе может красоваться создан препарат в целях лечения рака.
Учёные Института биофизики будущего МФТИ объединенно с коллегами разработали ненадеванный экспериментальный препарат держи основе наночастиц к прицельного уничтожения раковых клеток комбинацией фототерапии и таргетной химиотерапии. Лабораторные испытания нате животных показали, как эффективность разработки превышает 90% — таковский процент раковых клеток уничтожается в результате применения препарата. Об этом RT сообщили в бульдозер-службе Минобрнауки России. Разбирательство поддержано Минобрнауки и Российским научным фондом. Результаты опубликованы в Journal of Controlled Release.
Одна с важных задач, по-над решением которой работают учёные всего делов мира, — выковывание таргетных методов диагностики и лечения пустобрех. Традиционная химиотерапия имеет серьёзные побочные эффекты, так как препараты воздействуют никак не только на злокачественные, да и на здоровые красный товар пациентов. Чтобы прибавить негативные последствия терапии, полагается по штату поиск химических соединений, которые могут адресно взаимодействовать только-тол с онкомаркерами — рецепторами получи и распишись поверхности раковых клеток.
Т. е. отметили авторы работы, преимущественно перспективными платформами чтобы создания адресных средств онкотерапии являются непохожие наноструктуры. В основе разработанного препарата — наночастицы с биосовместимого сополимера получи основе молочной и гликолевой кислот (PLGA). Наночастицы с PLGA уже применяются в клинической практике по (по грибы) рубежом.

В такие наночастицы могут оказываться загружены, как в контейнеры, непохожие соединения, поэтому они обладают огромным потенциалом в качестве переносчика ради доставки препаратов нескованно к клеткам-мишеням. Одной с серьёзных проблем подле терапии рака является высокая адаптируемость опухоли к внешним воздействиям ради счёт более быстрого деления и мутаций раковых клеток. Следовательно важно применять присест) целый комплекс методик, разрушающих нарост, отмечают авторы исследования.
Во (избежание решения этой задачи биохимики совместили в новом препарате присест) две методики — классическую химиотерапию, а при этом целевого воздействия, а равно как фотодинамический подход. Фотодинамическая терапевтика применяется для лечения онкологии: в раковые текстиль вводится фотосенсибилизирующее сов, которое затем нагревается почти воздействием лазера, сие приводит к гибели клеток.
Авторы работы загрузили в полимерные наночастицы в то время как три агента: люминесцентный краситель для диагностики опухолей, фотосенсибилизатор чтобы фотодинамического воздействия и химиопрепарат. Биохимики как и модифицировали поверхность наночастиц изо PLGA таким образом, с целью они нацеливались в особые белковые рецепторы HER2. Повышенная яркость (синтез) этих белков характерна исполнение) опухолей молочной кандалы, с HER2 учёные также связывают риски развития метастазов и низкой выживаемости пациентов. Полученные наноструктуры учёные назвали таргосомами.
Лабораторные исследования сверху животных доказали непродуктивность таргосом. Совместное дело различных активных компонентов даёт синергетический действие и уничтожает более 90% раковых клеток.
«А именно комбинированное воздействие разными механизмами цитотоксичности — химиотерапевтическим препаратом иринотеканом и фотосенсибилизатором подле подключении внешнего источника ИК-излучения — позволило добиться такой высокой терапевтической эффективности возле лечении опухолей лабораторных грызунов», — рассказала RT патронесса лабораторией биохимических исследований канцерогенеза МФТИ Вира Шипунова.
Кроме того, изделие позволил визуализировать желвак и метастазы. По словам учёных, исполнение является отличным кандидатом нате использование в медицинских препаратах.
«Мультимодальные биосовместимые таргосомы являются препаратами медицины будущего, потому могут быть настроены для индивидуальные особенности каждого пациента. Сие реальная основа исполнение) разработки лекарств персонализированной медицины. Уникальное комбинирование в одной адресной платформе химиотерапии, диагностических и фототерапевтических свойств позволит доплестись высокой эффективности в терапии и диагностике различных видов онкологических заболеваний», — пояснила RT домогающийся лаборатории биохимических исследований канцерогенеза МФТИ Избранная Комедчикова.